Monosakarida digolongkan berdasarkan
jumlah atom
karbon yang dikandungnya (
triosa,
tetrosa,
pentosa,
heksosa,
dan
heptosa) dan gugus
aktifnya, yang bisa berupa
aldehida atau
keton. Ini kemudian
bergabung, menjadi misalnya aldoheksosa dan ketotriosa.Selanjutnya, tiap atom
karbon yang mengikat gugus hidroksil (kecuali pada kedua ujungnya) bersifat
optik aktif, sehingga
menghasilkan beberapa karbohidrat yang berlainan meskipun struktur dasarnya
sama. Sebagai contoh,
galaktosa adalah aldoheksosa, namun memiliki
sifat yang berbeda dari glukosa karena atom-atomnya disusun berlainan.

Fruktosa (bahasa Inggris: fructose, levulose), atau gula buah, adalah monosakarida yang
ditemukan di banyak jenis tumbuhan dan merupakan salah satu dari tiga gula darah penting
bersama dengan glukosa dan galaktosa, yang bisa langsung diserap ke aliran darah
selama pencernaan. Fruktosa ditemukan oleh kimiawan Perancis Augustin-Pierre Dubrunfaut pada tahun 1847. Fruktosa
murni rasanya sangat manis, warnanya putih, berbentuk kristal padat, dan sangat
mudah larut dalam air. Fruktosa
ditemukan pada tanaman, terutama pada madu, pohon buah, bunga, beri dan sayuran. Di tanaman, fruktosa
dapat berbentuk monosakarida dan/atau sebagai komponen dari sukrosa. Sukrosa merupakan molekul disakarida yang
merupakan gabungan dari satu molekulglukosa dan satu molekul fruktosa

Galaktosa
merupakan senyawa karbohidrat yang tergolong dalam monosakarida, termasuk juga
golongan heksosa karena mempunyai 6 atom C dalam molekulnya. Galaktosa merupakan salah satu monomer pembentuk
laktosa, senyawa ini dapat ditemukan pada susu. Galaktosa memiliki kemampuan menyerap di dalam
darah sehingga memiliki nilai glycaemic index yang lebih rendah dibandingkan
dengan sukrosa
1. MONOSAKARIDA
Monosakarida
ialah karbohidrat yang sederhana, yang berarti molekulnya hanya tersusun dari
beberapa atom karbon saja dan tidak dapat diuraikan dengan cara hidrolisis.
Umumnya monosakarida disusun oleh 3 samapai 7 atom karbon, dan jumlah atom
penyusunnya tersebut mempengaruhi pemanaan masing-masing monosakarida, yaitu :
1. Gula tiga karbon (Triosa)
Senyawa ini merupakan zat antara yang penting dalam lintasan
metabolik fotosintesis dan respirasi sel. Yang termasuk ke dalam golongan ini
adalah gliseraldehid dan dihidroksiaseton.
2. Gula empat karbon (Tetrosa)
Gula ini tidak banyak ditemui, walaupun beberapa bentuk
berperan dalam proses fotosintesis dan respirasi.
3. Gula lima karbon (Pentosa)
Senyawa ini sangat penting dalam fotosintesis dan respirasi.
Dua jenis pentose (ribose dan deoksiribosa) juga membentuk unsure pembangun
utama untuk asam nukleat, yang penting bagi semua kehidupan.
4. Gula enam karbon (heksosa)
Gula ini sering ikut serta dalam tahap respirasi dan
fotosintesis dan menjadi bangun utama dari banyak macam karohidrat lain
termasuk pati dan selualosa. Kunci dari heksosa adalah glukosa dan fruktosa.
5. Gula tujuh-karbon (heptosa)
Salah satu jens heptosa adalah zat antara dalam fotosintesis
dan respirasi. Jika tidak dalam bentuk itu, gula ini jarang didapati.
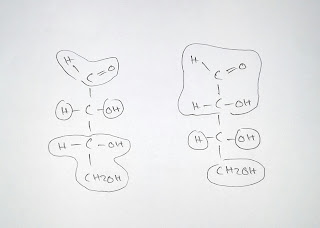
Berikut rumus struktur monosakarida :
Karbohidrat
yang paling sederhana adalah aldehida atau keton mempunyai dua atau lebih gugus
hidroksi. Monosakarida yang paling kecil adalah gliseraldehida dan
dihidroksiaseton senyawa-senyawa ini adalah triosa. Gliseraldehida mengandung
gugus aldehida mempunyai karbon asimetrik tunggal jadi terdapat dua streoisomer
dari aldose tiga karbon ini, D-gliseraldehida dan L-gliseraldehida. Sedangkan
dihidroksi aseton adalah ketosa karena mengandung gugus keton.